Microbiota intestinale e inflammaging
Fra i fattori che influenzano i processi di infiammazione è incluso il microbiota intestinale. Questa popolazione di microbi, 10 volte più numerosa rispetto al numero di cellule umane nell'organismo, comprende più di 50 phylum di batteri diversi e vive concentrata principalmente nel colon, dove svolge il ruolo di mediatore dei rapporti tra alimentazione, metabolismo e sistema immunitario. Il microbiota intestinale riveste un ruolo fondamentale nell'inflammaging
Far far away, behind the word mountains, far from the countries Vokalia and Consonantia, there live the blind texts. A small river named Duden flows by their place and supplies it with the necessary regelialiaIl microbiota intestinale riveste un ruolo fondamentale nell'inflammaging.
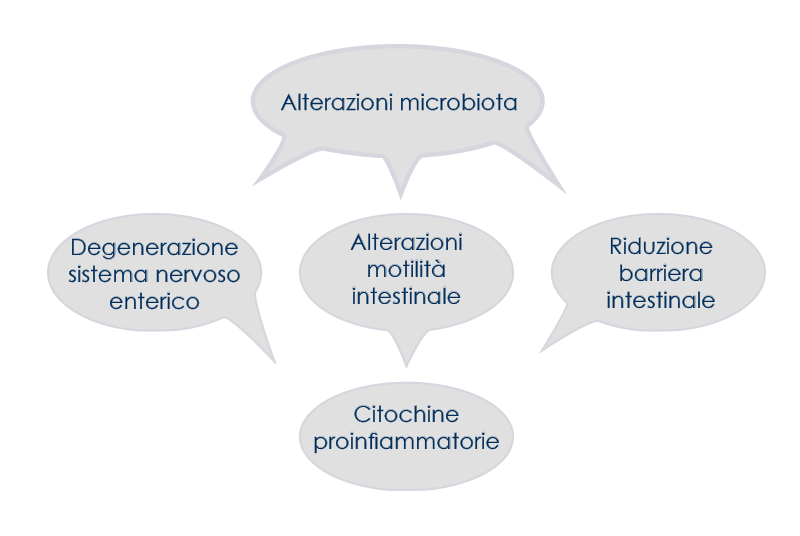
Le variazioni della sua composizione e della sua stabilità che si verificano durante l'invecchiamento sono associate alla degenerazione del sistema nervoso enterico, ad alterazioni della motilità intestinale e alla riduzione dell'efficienza della barriera difensiva costituita dalla mucosa intestinale; la maggior parte delle malattie associate all'invecchiamento è correlata a cambiamenti di questo tipo, a loro volta associati all'aumento dei livelli di citochine proinfiammatorie come le interleuchine (IL) 6 e 8.
In generale, durante l'invecchiamento il microbiota intestinale tende a perdere la capacità di fermentare i carboidrati, mentre riesce a fermentare meglio le proteine. La sua diversità tende a diminuire e alcune specie prendono il sopravvento rispetto ad altre.
Fra i microbi che tendono ad aumentare sono inclusi i Proteobacteria; particolarmente abbondanti nei centenari, questi batteri rappresentano in genere una componente minoritaria del microbiota intestinale, ma in alcune circostanze possono proliferare inducendo anche delle patologie.
Anche i livelli di Akkermansia muciniphila, un microbo in grado di degradare la mucina (uno dei componenti della barriera intestinale), aumentano. I bifidobatteri (fermenti lattici alleati della salute) e i microbi che producono butirrato (un acido grasso a catena corta che regola mediatori dell'infiammazione come il Tumor Necrosis Factor α, l'ossido nitrico e le interleuchine 6 e 10 e che protegge dalle malattie infiammatorie intestinali) tendono invece a diminuire.
Il rapporto tra Firmicutes e Bacteriodetes si inverte; a predominare sono questi ultimi, e anche la proporzione relativa di diversi gruppi di Firmicutes cambia significativamente.

Alcuni di questi cambiamenti sono influenzati dallo stile di vita – per esempio da un'alimentazione meno varia rispetto a quella che si segue in età meno avanzata, oppure dal non raro aumento del consumo di zuccheri e di cibi ricchi di grassi e dalla riduzione di quello di alimenti di origine vegetale. La risposta immunitaria scatenata da alimenti che promuovono uno stato infiammatorio può a sua volta accentuare le variazioni del microbiota, portando all'instaurarsi di un circolo vizioso. Ma i fattori esterni che possono causare variazioni del microbiota sono anche altri, per esempio l'assunzione di farmaci (in particolare di antibiotici) e il fatto di vivere in strutture di ricovero.
Altri cambiamenti del microbiota, come la riduzione di alcuni microbi produttori di butirrato e l'aumento di specie associate all'infiammazione come l'Escherica coli, risentono invece meno dell'influenza di fattori esterni all'organismo. Queste variazioni potrebbero rappresentare le caratteristiche fondamentali del microbiota nella terza età. Infine, durante l'invecchiamento la permeabilità intestinale tende ad aumentare, e alterazioni fisiche dell'epitelio di rivestimento dell'intestino associate all'aumento dell'interleuchina 6 potrebbero giocare un ruolo nelle disbiosi e dell'inflammaging.
Il microbiota intestinale è stato coinvolto sia nell'induzione sia nel mantenimento dell'inflammaging. L'aumento di Proteobacteria è stato per esempio associato a un'infiammazione locale, a livello dell'intestino, e sistemica, con attivazione dei linfociti T.
Secondo alcuni studi la presenza, nel sangue, di molecole derivanti dal microbiota intestinale può attivare i macrofagi verso uno stato proinfiammatorio che può promuovere l'aterosclerosi e che è associato allo sviluppo non solo di malattie cardiovascolari ma anche di demenza vascolare. Altre ricerche hanno svelato che le variazioni nei livelli di citochine e di acidi grassi a catena corta associati a cambiamenti nel microbiota intestinale possono influenzare l'attività del sistema nervoso centrale, dando così il loro contributo al declino cognitivo. E la risposta proinfiammatoria stimolata dal lipopolisaccaride (la tossina batterica associata alla sepsi) promuove la produzione di proteina beta-amiloide, fornendo la prova di un possibile legame tra il microbiota intestinale e la malattia di Alzheimer.